Substâncias húmicas são uma mistura complexa, dispersa e heterogênea[1] de vários compostos orgânicos sintetizados a partir de restos de matéria orgânica decomposta por microorganismos.[2] Portanto, as substâncias húmicas existem em uma grande variedade de estruturas e composições químicas.[3] Todavia, uma característica comum às substâncias húmicas é a presença de anéis benzênicos. O termo "substâncias húmicas" foi cunhado por cientistas do solo na década de 1930, bem como suas subdivisões operacionais: ácidos fúlvicos, ácidos húmicos e humina. A soma de ácidos fúlvicos e húmicos é citada por alguns autores como compostos húmicos.[2]
Os biomonômeros, que são, por exemplo, açucares e aminoácidos produzidos a partir do metabolismo de microorganismos unem-se quimicamente formando substâncias húmicas,[3] que não são hidrolizáveis[2] e são mais resistentes à degradação.[3] Por esse motivo as substâncias húmicas acumulam-se em solos, corpos aquáticos e nos depósitos fósseis de carvão mineral, hulha e turfa. Estima-se que elas sejam a maior fração dos compostos orgânicos naturais nesses compartimentos.[4] Em solos, as substâncias húmicas compôem o húmus, notadamente conhecido por aumentar a fertilidade do terreno.[5] Também são responsáveis por aumentar a produção biológica em corpos de água.[4]
Ao processo de síntese das substâncias húmicas dá-se o nome de humificação.[5] As substâncias húmicas, ao serem soterradas por camadas sedimentares, podem ser consumidas por microorganismos ou sofrer alterações e transformar-se em querogênio, material orgânico insolúvel precursor do petróleo, gás natural e carvão mineral.[2] Elas apresentam coloração amarelada a marrom dependendo de seu tipo, concentração e estágio de degradação da matéria orgânica.[5]
Classificação e técnicas de separação
As substâncias húmicas são divididas em três diferentes grupos: ácidos fúlvicos, ácidos húmicos e humina. Estas subdivisões baseiam-se em técnicas de separação das substâncias húmicas.
Separação em solo e sedimento
A separação de substâncias húmicas presentes em solo e sedimento é feita a partir da adição de solução de hidróxido de sódio e pirofosfato de sódio à amostra.[carece de fontes] O resíduo insolúvel desta fase é a humina. Posteriomente é utilizado um ácido forte que precipita os ácidos húmicos, enquanto os ácidos fúlvicos permanecem em solução.[2] Dessa forma:
- Ácidos fúlvicos representam fração das substâncias húmicas que é solúvel em ácido (pH < 2)
- Ácidos húmicos representam a fração das substâncias húmicas que é insolúvel em ácido (pH < 2)
- Humina representa a fração das substâncias húmicas que é insolúvel em base (NaOH)
Separação em água
Para a separação de compostos húmicos (ácidos fúlvicos e ácidos húmicos) dissolvidos em água é necessária uma etapa anterior àquela descrita acima: extrai-los do meio aquoso utilizando uma resina.[carece de fontes] Os compostos húmicos ficam adsorvidos nessa resina e, posteriormente, são lavados com solução alcalina. Dessa forma, cria-se uma outra definição operacional para compostos húmicos: aqueles que ficam adsorvidos em resinas não-iônicas com macroporos (ou procedimento equivalente).[1] Compostos húmicos podem ser estudados indiretamente como componentes da matéria orgânica cromofórica dissolvida ou matéria orgânica refratária.[6]
Composição, síntese e estrutura
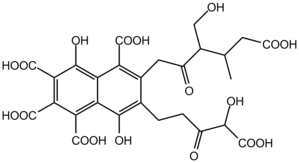
As substâncias húmicas apresentam massa molecular de 500 a 5000 Da.[carece de fontes] Sua composição química é constituída por aproximadamente 50% de carbono, 4-5% de hidrogênio, 35-40% de oxigênio e 1-2% de enxofre e fósforo,[1] dentre outros elementos químicos como os metais cobre, mercúrio e urânio.[2][3] Os principais grupos funcionais encontrados nas substâncias húmicas são ácido carboxílico, álcool e fenil.[1] A grande variação no grau de polimerização e no número de cadeias laterais e radicais que podem ser encontrados nas substâncias húmicas faz com que não existam duas moléculas idênticas.
É comum a ocorrência de compostos nutricionalmente pobres dentro das substâncias húmicas, como alguns derivados de plantas, parede celular e membrana de microorganismos.[3] Exemplos são os derivados de lignina, vegetais terrestres e celulose.[3] Também são encontrados nesses compostos fragmentos de polissacarídeos, melanina, proteínas, lipídios, ácidos nucleicos, entre outros.[4]
Compostos livres e hidrolizáveis são rapidamente consumidos por microorganismos. O resíduo desses compostos, que não é diretamente utilizado por microorganismos para a obtenção de energia, é incorporado em substâncias húmicas. Hidrocarbonetos não são afetados durante esse processo de humificação, pois não possuem grupos funcionais para realizar reações de polimerização embora possam ser encontrados adsorvidos ou unidos por pontes de hidrogênio às substâncias húmicas.[2]
Existe uma tendência de ácidos fúlvicos tornarem-se ácidos húmicos e, eventualmente, humina à medida que vão perdendo seus grupos funcionais. Este é o processo mais significativo para a formação de humina na maioria dos ambientes nos quais ácidos fúlvicos e húmicos estão presentes.[2] Em geral, quanto mais degradação uma molécula de substância húmica sofre, mais ligações cruzadas, aromaticidade, ciclização, esferificação e depleção de nitrogênio irá ocorrer nessa molécula.[3]
Em geral, compostos húmicos possuem uma “dorsal” ou núcleo formado por uma unidade de alquila ou benzeno. Oxigênio e nitrogênio presentes em outras cadeias ligam-se a esse núcleo, anexando suas cadeias. Os principais grupos funcionais que participam das reações são ácido carboxílico, álcool, cetona e fenol. As principais reações químicas que fazem parte da humificação são a oxidação, a polimerização e condensação.[3]
Origem e ocorrência em compartimentos ambientais
Solos
As substâncias húmicas ocorrem no solo como a fração mais estável da matéria orgânica. Como consequência dessa estabilidade, elas constituem a reserva orgânica do solo. Os ácidos húmicos em solos são gerados sob condições oxidantes.[1] Sua origem está ligada à atividade de enzimas e microrganismos presentes no material orgânico incorporado ao solo, cuja principal fonte é constituída pelos resíduos vegetais.
A condensação oxidativa de fenóis é um processo importante para a humificação no solo.[carece de fontes] A adição de compostos nitrogenados ocorre via polimerização randômica de radicais nitrogenados.[2] De forma geral, carbono aromático é predominante nas moléculas. Os compostos húmicos de solo possuem uma estrutura central aromática bem definida, com cadeias alifáticas ligadas à mesma.[carece de fontes] A grande quantidade de anéis aromáticos deve-se provavelmente aos restos de lignina produzida por plantas terrestres.[3]
Em comparação com compostos húmicos marinhos, as substâncias húmicas presentes no solo possuem maior acidez total, um fenômeno causado pela aeração.[carece de fontes] Com o ar penetrando no solo, mais grupos carboxila são anexados em comparação com outros grupos carbonila. Adicionalmente, as substâncias húmicas do solo contêm mais cadeias policíclicas e polifenólicas e menor concentração de hidrogênio e nitrogênio do que as substâncias húmicas marinhas, embora grupos funcionais totalizem 50 a 60% dos ácidos fúlvicos.[3]
No solo, as substâncias húmicas podem se adsorver a colóides argilosos (formando complexos argilo-húmicos) ou reagir com o íon Ca2+ (tornando-se mais resistentes à biodegradação).[carece de fontes] Há casos em que a permanência da fração húmica no solo é muito curta, como observado em solos tropicais que apresentam baixo teor de argila.[carece de fontes] Os teores de substâncias húmicas também podem ser reduzidos no solo devido a práticas agrícolas que comumente favorecem a monocultura e estimulam maior atividade microbiana e enzimática.
Sedimentos
Em sedimentos superficiais e jovens, substâncias húmicas compõem 75 a 90% da matéria orgânica, enquanto lipídios e hidrocarbonetos ocorrem em frações menores, assim como os monômeros gerados pela degradação de proteínas e polissacarídeos (aminoácidos e monossacarídeos, respectivamente).[2] Com o aumento da profundidade e a ocorrência dos processos de diagênese recente, muita matéria orgânica é consumida por microorganismos, inclusive substâncias mais resistentes à degradação como hidrocarbonetos, terpenos, esteróis, pigmentos e substâncias húmicas.[2]
Nos primeiros dez metros de profundidade de camada sedimentar, ácidos fúlvicos e húmicos compõem de 10 a 70% de toda a matéria orgânica, com os maiores valores encontrados em lamas de deltas estuarinos.[carece de fontes] Nesse pacote sedimentar, ocorre o rompimento de ligações peptídicas nos compostos húmicos e a diminuição dos teores de nitrogênio.[2] Na escala de centenas de metros de profundidade dentro da camada sedimentar, os teores de oxigênio em compostos húmicos diminuem, principalmente pela perda de grupos ácido carboxílico.[carece de fontes] As reações de perda de funções hidrofílicas, condensação, dentre outras, acarretam na geração de ácidos húmicos a partir de ácidos fúlvicos. Humina é formada a partir de ácidos húmicos em uma escala de milhões de anos. A mudança é visível à medida em que os compostos passam a ter uma coloração mais escura.[2]
Mares e oceanos
Nos mares e oceanos, substâncias húmicas representam a maior parte da matéria orgânica natural, seja nas frações dissolvida ou particulada. Na fração dissolvida, por exemplo, 40 a 60% da matéria orgânica é constituída por substâncias húmicas.[1]
As propriedades físico-químicas dos compostos húmicos dependem das fontes de matéria orgânica a partir das quais são originadas. Ocorre também transporte de compostos húmicos continentais para as regiões costeiras. Em áreas de grande aporte fluvial, materia orgânica continental é a fonte majoritária disponível para a humificação.[2] Nessas regiões, ácidos fúlvicos e húmicos são abundantes.[2][3] Em média, no oceano global, há mais compostos húmicos gerados a partir de matéria orgânica continental alóctone do que autóctone, provavelmente porque a maior parte da produção biológica marinha ocorre em ambientes costeiros.[2]
Apesar de compostos húmicos apresentarem resistência à degradação, em locais longe de margens continentais ou próximo ao continente antártico, a matéria orgânica livre disponível é quase toda autóctone.[2] A ausência de acúmulo dessas substâncias longe das margens continentais sugere que há mecanismos de quebra de compostos húmicos, podendo envolver organismos vivos. A degradação fotoquímica pode quebrar os compostos húmicos em moléculas menores e liberar gases como o monóxido e o dióxido de carbono durante a oxidação.[3]
Material orgânico oriundo do continente contém grandes quantidades de restos de lignina e celulose, característicos de plantas terrestres. Matérial autóctone marinho é oriundo principalmente do fitoplâncton. No oceano, os compostos húmicos fazem parte do grande grupo dos compostos refratários, nos quais é comum encontrar restos de parede celular e membrana de fitoplâncton.[3]
Compostos húmicos marinhos possuem menos constituintes fenólicos e aromáticos do que os compostos húmicos de solos.[carece de fontes] A razão entre hidrogênio e carbono varia de 1 a 1,5, resultado da abundância de cadeias alifáticas e anéis alicíclicos em ácidos húmicos marinhos.[2][3] O nitrogênio é mais abundante em compostos húmicos marinhos devido à maior quantidade de organismos marinhos que possuem altos teores de desse elemento.[3] Enxofre também é comparativamente mais abundante.[2]
Os processos de policondensação ocorrem sob condições aeróbias e anaeróbias nos oceanos,[2] embora em condições anaeróbias moléculas muito condensadas ocorram em menor frequência. Há também nesses casos um acúmulo de grupos carbonila.[3] As ligações peptídicas ocorrem frequentemente em compostos húmicos marinhos, principalmente em águas rasas. Carboidratos e aminoácidos podem reagir rapidamente e produzir um policondensado estruturalmente muito próximo aos compostos húmicos.[2]
Ver também
Referências
- ↑ 1,0 1,1 1,2 1,3 1,4 1,5 Thurman, E. M. (1985). «Aquatic Humic Substances». Organic Geochemistry of Natural Waters. [S.l.]: Springer Netherlands. ISBN 978-94-010-8752-0. doi:10.1007/978-94-009-5095-5
- ↑ 2,00 2,01 2,02 2,03 2,04 2,05 2,06 2,07 2,08 2,09 2,10 2,11 2,12 2,13 2,14 2,15 2,16 2,17 2,18 2,19 2,20 Tissot, Bernard P.; Welte, Dietrich H. (1984). Petroleum Formation and Occurrence 2 ed. [S.l.]: Springer-Verlag. ISBN 0-387-13281-3
- ↑ 3,00 3,01 3,02 3,03 3,04 3,05 3,06 3,07 3,08 3,09 3,10 3,11 3,12 3,13 3,14 3,15 Libes, Susan M. (2009). Introduction to Marine Biogeochemistry 2 ed. [S.l.]: Elsevier. ISBN 978-0-12-088530-5
- ↑ 4,0 4,1 4,2 «IHSS - What are Humic Substances?». www.humicsubstances.org. Consultado em 16 de janeiro de 2016
- ↑ 5,0 5,1 5,2 Waksman, Selman A. (1936). Humus. Origin, chemical composition and importance in nature. [S.l.]: The Williams & Wilkins Company
- ↑ Ronei Ezequiel da Paixão (9 de dezembro de 2003). «Avaliação química e espectroscópica do grau de maturidade do composto de resíduos de podas e lodo de esgoto industrial em escala de laboratório» (PDF). Acervo Digital da Universidade Federal do Paraná (UFPR). Consultado em 13 de julho de 2018





 " class="attachment-atbs-s-4_3 size-atbs-s-4_3 wp-post-image" alt="O que estudar para o enem 2023">
" class="attachment-atbs-s-4_3 size-atbs-s-4_3 wp-post-image" alt="O que estudar para o enem 2023"> " class="attachment-atbs-s-4_3 size-atbs-s-4_3 wp-post-image" alt="Qual melhor curso para fazer em 2023">
" class="attachment-atbs-s-4_3 size-atbs-s-4_3 wp-post-image" alt="Qual melhor curso para fazer em 2023"> " class="attachment-atbs-s-4_3 size-atbs-s-4_3 wp-post-image" alt="Enem: Conteúdos E Aulas On-Line São Opção Para Os Estudantes">
" class="attachment-atbs-s-4_3 size-atbs-s-4_3 wp-post-image" alt="Enem: Conteúdos E Aulas On-Line São Opção Para Os Estudantes"> " class="attachment-atbs-s-4_3 size-atbs-s-4_3 wp-post-image" alt="Como Fazer Uma Carta De Apresentação">
" class="attachment-atbs-s-4_3 size-atbs-s-4_3 wp-post-image" alt="Como Fazer Uma Carta De Apresentação"> " class="attachment-atbs-s-4_3 size-atbs-s-4_3 wp-post-image" alt="Como Escrever Uma Boa Redação">
" class="attachment-atbs-s-4_3 size-atbs-s-4_3 wp-post-image" alt="Como Escrever Uma Boa Redação"> " class="attachment-atbs-s-4_3 size-atbs-s-4_3 wp-post-image" alt="Concurso INSS edital 2022 publicado">
" class="attachment-atbs-s-4_3 size-atbs-s-4_3 wp-post-image" alt="Concurso INSS edital 2022 publicado">


