| Mycobacterium | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Classificação científica | |||||||||||||
| |||||||||||||
| Espécies | |||||||||||||
Mycobacterium ou micobactéria é um gênero de actinobactérias bacilares, aeróbicas obrigatórias, imóveis e altamente patogênicas, que causam diversas doenças, entre as quais lepra, tuberculose e infeções por micobactérias não tuberculosas. Possuem a forma de bacilos retos ou levemente curvado, sem a presença de flagelos ou de cápsula, além de não ter formação do endosporo. Apesar das micobactérias não possuírem membrana externa e, por isso, se assemelharem às gram-positivas, seu alto teor lipídico confere diferenças estruturais importantes na parede. A presença de ácidos graxos no envelope confere uma álcool-ácido resistência (AAR) - retendo fucsina básica pela parede mesmo na presença de álcool e ácido durante a coloração de Gram. Microorganismo intracelulares, que infectam e proliferam-se dentro de macrófagos.
As manifestações clínicas de infecções micobacterianas decorrem da resposta imunológica do hospedeiro à infecção e aos antígeos que portam. Possuem inúmeras resistências a antibióticos típicos e exigem tratamentos de muitas semanas, meses ou anos. Normalmente administrado mais de um antibiótico, já que algumas cepas já apresentam resistência antimicrobiana considerável. [1]
Parede celular
Diferente de outras bactérias gram-positivas ou gram-negativas, as micobactérias possuem peptideoglicano com ácido N-glicolilmurâmico em vez de ácido N-acetilmurâmico. A parede celular é constituída de cerca de 60% de ácidos micólicos (ácidos graxos de cadeia longa incomum), covalentemente ligados ao polissacarídeo que compõe a parede. A presença de alguns lipídeos livres com epítopos passiveis de reconhecimento pelo hospedeiro não estão covalentemente associados ao esqueleto basal. Possuem proteínas de membrana formadoras de canais catiônicos (porinas), que controlam a difusão de moléculas hidrofílicas. A Mycobacterium tuberculosis possui uma das paredes mais permeáveis a agentes antimicrobiano hidrofílicos. [1] A singularidade da parede permite que o microorganismo sobreviva dentro de macrófagos - que normalmente aniquilam patógenos fagocitados - facilitando a agregação bacteriana e tornando-as mais resistentes a muitos desinfetantes químicos, o que dificulta sua prevenção.
Coloração
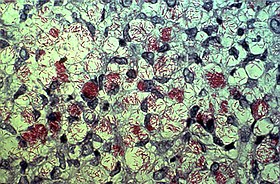
O alto teor lipídico das micobactérias confere à esta a álcool-ácido resistência, que impede a coloração das bactérias pela técnica de Gram, normalmente utilizada. Entretanto, se a porção lipídica for removida com etanol alcalino, a bactéria perde a característica de álcool-acido resistência, permitindo que sua coloração assemelhe-se às gram-positivas. A técnica de Ziehl-Neelsen é eficaz com essas bactérias, utilizando uma mistura de fucsina com fenol, envolvendo aquecimento na própria lâmina até que gere vapor. O diferencial dessa mistura é o fenol, que aumenta a absorção da fucsina nos lipídios (ocorrerá ligação do NH2+ da fucsina com o COO- do ácido micólico). Após essa aplicação, o esfregaço é lavado e tratado com álcool-ácido, sendo lavado mais uma vez para ser corado com azul de metileno, realizando o papel de contraste. O resultado é a coloração em vermelho aos acidorresistentes, e o restante em azul. [2]
Meio de cultura
Possui um meio desenvolvido especialmente para seu plaqueamento, o meio Löwenstein–Jensen (LJ), que é utilizado principalmente para o cultivo da Mycobacterium tuberculosis. Diferenças entre as espécies englobam mudanças na temperatura ótima de cultivo e tempo médio de crescimento.
COMPOSIÇÃO (g/L)
L-Asparagina: 3.60
Fosfato monopotássico: 2.40
Sulfato de magnésio: 0.24
Citrato de magnésio: 0.60
Amido de batata, solúvel: 30.00
Verde malaquita: 0.400
Essa é a composição basal, comprada em forma de um pó azul esverdeado. A ele, devem ser acrescentados 12mL de glicerol e 1000mL de emulsão de ovo. Nesse momento o meio adquire uma cor verde azulada pálida, e um pouco opaca.
A l-asparagina e o amido de batata são fontes de nitrogênio e vitaminas. Sulfato de magnésio e fosfato monopotássico agem como fatores de crescimento, e o glicerol e a emulsão de ovo fornecem ácidos graxos e aminoácidos e são fonte de carbono. O verde malaquita é composto que impede a contaminação a cultura por fungos e outros microrganismos, garantindo uma cultura pura.
Esse meio é muito importante para o diagnóstico precoce da tuberculose, mas seu grande problema se da pelo fato de que as colônias demoram para serem formadas devido ao crescimento lento da bactéria (colônias visíveis de 2 a 20 dias em temperatura ótima). Isso dificulta muito a rapidez de diagnóstico, e por isso técnicas alternativas são bastante pesquisadas e exploradas. Por não serem nem gram-positivas nem gram-negativas, podem ser cultivadas com antibióticos para esses dois tipos de bactérias, o que minimiza e evita contaminações.
A Mycobacterium leprae não é cultivada nesse meio ou em qualquer outro, sendo utilizado modelos experimentais para análise da hanseníase. O uso de tatu selvagem em laboratórios como modelo experimental ainda é o mais adequado. [3][4]
Metabolismo
Devido à baixa velocidade de crescimento e a dificuldade de cultura dessas bactérias, o metabolismo dessas bactérias não é definido para todas as espécies. Suas necessidades nutricionais englobam:
- fonte de carbono orgânica
- fonte de nitrogênio (NH4+)
- elementos inorgânicos usuais (Mg2+ , SO4 2 ~, K + , PO4 3 ", Fe3 +, etc.).
Dentre as principais bactérias patogênicas, a Mycobacterium tuberculosis usa como principal fonte de carbono o colesterol e esteroides derivados de sua degradação como metabólitos adicionais. Uma via de regulação da ativação dos genes que participam do catabolismo do colesterol inicia-se com sua oxidação, até eventualmente alimentar o ciclo de Krebs (TCA Cicle) ou ser usado para o anabolismo da bactéria.[5]
A Mycobacterium leprae usa principalmente os lipídios como fonte de carbono. Eles também são oxidados e eventualmente servem de substrato para o ciclo de Krebs, que enfim fornece ATP para a bactéria.Como a M. leprae só cresce em hospedeiros específicos e não cresce em meios de culturas padrão para micobactérias, elas não produzem todos os metabólitos necessários ao seu crescimento. Entretanto, como seu crescimento ocorre em hospedeiros específicos, é de difícil determinação quais nutrientes ela precisa utilizar do meio em que se encontra, sendo os mecanismos gerais de seu metabolismo ainda nebulosos. [6]
Micobactérias patogênicas
As infecções por micobactérias geralmente só afetam imunocomprometidos, sendo assintomáticas na grande maioria da população:[7]
Patógenos obrigatórios
- Mycobacterium tuberculosis: Tuberculose humana
- Mycobacterium bovis: Tuberculose humana/bovina
- Mycobacterium leprae: Hanseníase
Patógenos oportunistas
- Mycobacterium marinum: Infecções cutâneas profundas
- Mycobacterium ulcerans: Úlcera de Buruli
- Mycobacterium kansasii: Pneumonia similar a tuberculose
- Mycobacterium avium e Mycobacterium intracellulare simultâneos: Síndrome de Lady Windermere
- Mycobacterium africanum: Pneumonia similar a tuberculose
Biossegurança
Algumas bactérias do gênero Mycobacterium são causadoras de doenças extremamente perigosas, como a hanseníase e a tuberculose. A manipulação desses patógenos requer laboratórios equipados de acordo com os Níveis de Biossegurança (NB), requisitos padronizados para a manipulação de microrganismos patógenos.
Esses níveis são definidos de acordo com a classe de risco desses microrganismos (determinada pelo risco potencial oferecido ao individuo, à comunidade e ao meio ambiente) e ao tipo de manipulação que será realizada. [8]
CLASSE DE RISCO 1: todas as Mycobacterium não incluídas em outras classes de risco.
CLASSE DE RISCO 2: M. leprae, M. asiaticum, M. avium, M. bovis BCG vacinal, M. intracellulare, M. chelonae, M. fortuitum, M. kansasii, M. malmoense, M.marinum, M. paratuberculosis, M. scrofulaceum, M. simiae, M. szulgai,M. xenopi
CLASSE DE RISCO 3:M. bovis (exceto a cepa BCG) e M. tuberculosis [9]
O número da classe de risco não corresponde ao NB necessariamente. Existem micobactérias,como a M.smegmatis, que são da classe de risco 1 e correspondem ao NB 1, e a M.leprae, que é da classe 2 e corresponde ao NB 2. Por outro lado, existem casos como a M.tuberculosis, que faz parte da classe de risco 3, mas pode corresponder ao NB 2 ou 3, dependendo do tipo de manuseio a ser realizado. [10]
Antibióticos
Devido a característica de álcool-ácido resistência, as micobactérias possuem antimicrobianos específicos para o tratamento de enfermidades causadas pelas bactérias patogênicas. Os casos de resistência aos fármacos pela micobactéria ocorre devido às mutações espontâneas que ocorrem nas replicações dessas bactérias - não envolvendo plasmídeos e transposons (elementos móveis) como ocorre na maioria das bactérias resistentes a antibióticos.
A rifampicina é um importante antibiótico no tratamento da tuberculose, hanseníase e outras doenças causadas por micobactérias. É um composto semi-sintético produzido a partir da rifampicina B, que é obtida comercialmente pela fermentação a partir do Streptomyces mediterranei. Pertencente à família dos antibióticos ansamicinas, é um antibiótico bactericida que se liga a subunidade beta da RNA polimerase e inibe a transcrição gênica da micobactéria por bloqueio da RNA-polimeras dependente de DNA. Isso impede a síntese de RNA mensageiro (mRNA), produzindo morte celular. O mecanismo de resistência a esse fármaco resulta de mutações na região central do gen rpoB, que codifica a subunidade β da RNA-polimerase . As mutações modificam a estrutura desta enzima, fazendo com que a RMP perca a capacidade de bloqueá-la, liberando a síntese de mRNA.
Observação importante: A utilização da rifampicina em pacientes portadores de HIV pode promover interações farmacológicas do sistema hepático e intestinal com a maioria dos anti-retrovirais utilizados, o que pode provocar uma redução significativa dos níveis plasmáticos dos mesmos. Esse fato pode levar à diminuição da eficácia e ao aumento do risco de desenvolvimento de resistência do vírus HIV ao esquema de medicamentos anti-retrovirais. Assim, é necessário a utilização de processos alternativos, sem a presença da rifampicina.
A isoniazida, medicamento mais conhecido no tratamento da tuberculose devido a sua alta especificidade e também aquele com maior frequência de ocorrência de resistência, foi descoberto em 1952. O gene katG codifica a enzima catalase-peroxidase, importante no metabolismo do bacilo. Esta enzima ativa a isoniazida, produzindo radicais reativos de oxigênio e radicais orgânicos que inibem a formação de ácidos micólicos da parede bacilar e produzem dano no DNA.O gene inhA codifica a enzima carreadora de enoil (acil redutase) NADH dependente, que é importante na síntese de ácidos micólicos. Um dos produtos da isoniazida ativada (o radical acil isonicotínico) liga-se à NADH e impede a atividade da enzima, resultando na morte da bactéria por interferência na síntese do ácidos micólicos. As micobactérias que apresentam resistência à Isoniazida geralmente se livram dessa enzima que ativa o medicamento ou apresentam mutações, como no gene katG há diminuição da ação da catalase. A mutação estrutural do gene inhA faz com que a enzima modificada perca afinidade pela NADH. Ambas mutações resultam em resistência É bacteriostático e é utilizado ate hoje, embora algumas linhagens já apresentem resistência ao medicamento.
A Pirazinamida é um antibiótico muito utilizado no tratamento da Tuberculose. Não se sabe o exato mecanismo de ação pelo qual a pirazinamida inibe o crescimento da Mycobacterium tuberculosis (Mtb), porém sabe-se que ela tem atividade altamente específica contra essa micobactéria, não exercendo qualquer efeito sobre as outras. É provável que a quebra da molécula da pirazinamida através de sua enzima pirazinamidase-nicotinamidase nessas micobactérias produz ácido pirazinoico, a forma ativa da droga, em pH ácido. A atividade defeituosa da pirazinamidase, devido a mutações no pncA, é a principal causa de resistência a pirazinamida.
Etambutol é um tuberculostático sintético e micobacteriostático que não possui efeito sobre outras bactérias. O exato mecanismo não está totalmente conhecido, mas parece inibir a síntese de metabólitos, levando ao dano ao metabolismo celular, parada da multiplicação e morte celular. É ativo apenas quando a célula estiver em divisão.A resistência desenvolve-se in vivo, quando administrada na ausência de outra droga eficaz.
A Dapsona é um medicamento utilizado para diversos problemas que afetam a pele. Muito usado no tratamento da Hanseníase, ele age inibindo a síntese de ácido fólico, pela competição com o ácido para-amino-benzóico (PABA) na bactéria, devido a sua similaridade estrutural. Com isso há inibição na formação de DNA e RNA, impedindo a replicação e transcrição do mesmo, afinal o PABA é essencial na síntese de ácido fólico e consequentemente para a síntese de purinas, envolvidas diretamente na formação de DNA e RNA. A resistência à dapsona é associada às mutações nos códons 53 e 55 no gene folp1, gene relacionado à biossíntese de folato.
Clofazimina: Ela tem ação bacteriostática com relação ao bacilo de Hansen, ou seja inibe o crescimento micobacteriano, e, também segundo alguns, uma ação antinflamatória. Ainda não foi demonstrada resistência do Mycobacterium leprae à clofazimina e pouco se sabe sobre seu mecanismo de ação exato.
A associação da dapsona, rifampicina e clofazimina é eficaz no tratamento da hanseníase multibacilar, entretanto a dapsona é responsável por inúmeros efeitos colaterais, tais como anemia hemolítica, metahemoglobinemia, erupções cutâneas, neuropatias, agranulocitose, entre outras. Por isso tratamentos alternativos, como a substituição da dapsona pela ofloxacina, ou a utilização do sistema ROM (rifampicina, ofloxacina e minociclina) estão sendo aplicados atualmente.
A ofloxacina, uma droga do grupo das fluoroquinolonas, que possui grande espectro de ação, inibe a replicação do DNA devido à ligação com a subunidade A da DNA girase no gene gyrA. Mutações associadas com o gene gyrA são comumente relatadas em micobactérias. As mutações identificadas até o momento no gene gyrA encontram-se no códon 89 e no códon 91. Também substituições de aminoácidos nos códons 91 e 94 são associadas com resistência às quinolonas.
As fluoroquilonas demonstraram poderosa atividade tuberculocida. Seu uso no tratamento da doença aumentou pelos recentes surtos de tuberculose resistente à diversas drogas. Entretanto, a utilização frequente das fluoroquinolonas no tratamento de diversas outras doenças infecciosas está gerando bactérias resistentes à essas drogas. Esse antibiótico pode desencadear uma vasta onda de efeitos colaterais debilitantes e portanto não devem ser usadas como primeira linha de tratamento.
O tratamento das doenças é mais eficaz quando administrado combinações de antibióticos, diminuindo a quase 0% as chances da bactéria possuir resistência aos dois medicamentos utilizados.
Micobacteriófagos
Micobacteriófagos são um tipo de vírus bacteriófago que têm micobactérias como hospedeiras. Originalmente isolados de Mycobacterium smegmatis ,[11] hoje são conhecidos mais de 4,200 micobacteriófagos, sendo mais de 500 completamente sequenciados.[12] Todos os micobacteriófagos conhecidos apresentam DNA de fita dupla e são classificados nas famílias Siphoviridae e Myoviridae.[13] Devido a uma especificidade de hospedeiro relativamente alta, micobacteriófagos podem ser usados para identificar espécies e linhagens de micobactérias. [14] Nos anos 1980, micobacteriófagos foram descobertos como ferramentas para a manipulação genética de micobactérias,[15][16] apresentando possibilidade para, no futuro, serem usados para identificar resistência [17] ou tratar infecções.[18]
Biotecnologia
O uso de micobactérias para a biotecnologia se volta principalmente para a cura de suas principais doenças, a tuberculose e a hanseníase.[19] A dificuldade natural para o tratamento dessas doenças, aliadas ao surgimento de cepas resistentes, requer técnicas de tratamento mais eficazes. Descobertas como a formação de biofilme protetor [20] e a função de uma recém descoberta fosforibosiltransferase,[21] um tipo de transferase, apresentam novos alvos para drogas antimicrobacterianas. A popularização do sistema CRISPR também mostra uma possível nova abordagem para a identificação e eliminação de micobactérias, em especial Mycobacterium tuberculosis.[22][23]
Espécies
- M. abscessus
- M. africanum
- M. asiaticum
- M. avium
- M. bovis
- M. canetti
- M. chelonae
- M. fortuitum
- M. gordonae
- M. haemophilum
- M. intracellulare
- M. kansasii
- M. lentiflavum
- M. leprae
- M. malmoense
- M. marinum
- M. microti
- M. phlei
- M. scrofulaceum
- M. smegmatis
- M. triplex
- M. tuberculosis
- M. ulcerans
- M. uvium
- M. xenopi
Referências
- ↑ 1,0 1,1 Trabulsi, Luiz Rachid (2008 - 5ª edição). Microbiologia. [S.l.]: Atheneu Verifique data em:
|ano=(ajuda) - ↑ Madigan, Michael T. (12ª edição). Microbiologia de Brock. [S.l.: s.n.] Verifique data em:
|ano=(ajuda) - ↑ «MeSH Pharmacological Classification»
- ↑ «Lowenstein Jensen (LJ) Medium : Composition, Preparation, Method of Use and Pictures»
- ↑ «Mycobacterium tuberculosis»
- ↑ «Mycobacterium leprae»
- ↑ «Gênero Mycobacterium spp» (PDF)
- ↑ «Níveis de Biossegurança»
- ↑ «Classificação de riscos de agentes biológicos» (PDF)
- ↑ «Manual de biossegurança para laboratórios da tuberculose» (PDF)
- ↑ «A Bacteriophage for Mycobacterium smegmatis.∗»
- ↑ «Actinobacteriophage Database»
- ↑ «Expanding the Diversity of Mycobacteriophages: Insights into Genome Architecture and Evolution»
- ↑ «Phage typing report of 125 strains of "Mycobacterium tuberculosis»
- ↑ «Introduction of foreign DNA into mycobacteria using a shuttle phasmid»
- ↑ WR, Jacobs Jr (2000). Molecular Genetics of the Mycobacteria. Washington: [s.n.]
- ↑ «Generation of a Novel Nucleic Acid-Based Reporter System To Detect Phenotypic Susceptibility to Antibiotics in Mycobacterium tuberculosis»
- ↑ «In vivo efficacy of phage therapy for Mycobacterium avium infection as delivered by a nonvirulent mycobacterium»
- ↑ Grange, J. M. World. Biotechnol. [S.l.: s.n.]
- ↑ «Targeting drug tolerance in mycobacteria: a perspective from mycobacterial biofilms»
- ↑ «A mycobacterial phosphoribosyltransferase promotes bacillary survival by inhibiting oxidative stress and autophagy pathways in macrophages and zebrafish»
- ↑ «Fighting tuberculosis with modern weapons»
- ↑ «Fighting against tuberculosis»






 " class="attachment-atbs-s-4_3 size-atbs-s-4_3 wp-post-image" alt="O que estudar para o enem 2023">
" class="attachment-atbs-s-4_3 size-atbs-s-4_3 wp-post-image" alt="O que estudar para o enem 2023"> " class="attachment-atbs-s-4_3 size-atbs-s-4_3 wp-post-image" alt="Qual melhor curso para fazer em 2023">
" class="attachment-atbs-s-4_3 size-atbs-s-4_3 wp-post-image" alt="Qual melhor curso para fazer em 2023"> " class="attachment-atbs-s-4_3 size-atbs-s-4_3 wp-post-image" alt="Enem: Conteúdos E Aulas On-Line São Opção Para Os Estudantes">
" class="attachment-atbs-s-4_3 size-atbs-s-4_3 wp-post-image" alt="Enem: Conteúdos E Aulas On-Line São Opção Para Os Estudantes"> " class="attachment-atbs-s-4_3 size-atbs-s-4_3 wp-post-image" alt="Como Fazer Uma Carta De Apresentação">
" class="attachment-atbs-s-4_3 size-atbs-s-4_3 wp-post-image" alt="Como Fazer Uma Carta De Apresentação"> " class="attachment-atbs-s-4_3 size-atbs-s-4_3 wp-post-image" alt="Como Escrever Uma Boa Redação">
" class="attachment-atbs-s-4_3 size-atbs-s-4_3 wp-post-image" alt="Como Escrever Uma Boa Redação"> " class="attachment-atbs-s-4_3 size-atbs-s-4_3 wp-post-image" alt="Concurso INSS edital 2022 publicado">
" class="attachment-atbs-s-4_3 size-atbs-s-4_3 wp-post-image" alt="Concurso INSS edital 2022 publicado">


